Személyre szabott rákterápia-tumormarkerek diagnosztikája
Personalized cancer therapy - tumor markers diagnostics
| Daganat típusTumour type | Érintett génekAffected genes | Célzott terápiás gyógyszerTargeted therapy drug | |
|---|---|---|---|
| EmlőrákBreast cancer | BRCA1, BRCA2, EGFR, PIK3CA, TP53 | ||
| Vastagbélrák | Colon cancer | BRAF, EGFR, HRAS, KRAS, NRAS, PIK3CA, TP53 | Cetuximab, Panitumumab |
| Tüdőrák | Lung cancer | BRAF, EGFR, KRAS, PIK3CA, KIT, TP53 | Erlotinib, Afatinib, Gefitinib, Osimertinib |
| Petefészekrák | Ovarian cancer | BRCA1, BRCA2, BRAF, EGFR, KRAS, NRAS, PIK3CA, KIT, TP53 | Olaparib |
| Gyomorrák | Gastric cancer | TP53, PIK3CA, PDGFRA | Imatinib, Sunitinib |
| Májrák | Hepatic cancer | BRAF, KRAS, PIK3CA, TP53 | |
| Prosztatarák | Prostate cancer | PIK3CA, TP53 |
A vastag- és végbél-, valamint nemkissejtes tüdőtumorok kezelésének jelenleg leghatékonyabb módja az úgynevezett EGFR jelátviteli útvonalat célozza meg annak gátlása által. A célzott terápia hatékonyságának felmérésére elengedhetetlen a KRAS, az NRAS, a BRAF és a PIK3CA gének vizsgálata, hiszen ha ezekben a génekben mutáció található, akkor az EGFR-gátló terápia a daganatsejtekre hatástalan marad, viszont az egész szervezetben előforduló mellékhatások megmaradnak és tovább gyengíthetik a szervezetet. Intézményünkben e vizsgálatok mindegyikét validált CE-IVD diagnosztikai kitekkel végezzük.
Currently, the most efficient treatment of colorectal and non-small cell lung cancers targets the so called EGFR signalling pathway via its inhibition. To assess the efficiency of targeted therapy, it is essential to analyse the KRAS, NRAS, BRAF, and PIK3CA genes, because if these genes contain mutations then the EGFR inhibitor therapy will not affect the tumour cells, but the side effects will remain, further weakening the patient. In our institute, we perform all of these assays using CE-IVD validated diagnostic kits.
A vizsgálatok friss és beágyazott (FFPE) tumorszövetből egyaránt elvégezhetőek.
The assays can be performed using both fresh and embedded (FFPE) tumour tissues.

Egy új korszak kezdete az orvostudományban
The beginning of a new era in medicine
A rákos betegségek kezelésében igazi újdonságként jelent meg az utóbbi évtizedben a személyre szabott, célzott daganatterápia.
A real novelty evolved in the treatment of cancer in the past decade: personalized, targeted tumour therapy.
Personalized because the analysis of certain tumour markers can determine which medicine should be used for a given patient.
Személyre szabott, mert a terápia során bizonyos tumormarkerek vizsgálatával meghatározható, mely gyógyszer kerüljön alkalmazásra az egyes betegeknél.
Célzott, mert az így ható gyógyszerek a hibás génekre, illetve azok hibás termékeire hatva nem direkt tumorpusztítást, hanem a kórosan fennálló sejtszaporodást vezérlő ingert oltják ki. Így sok esetben jelentős javulás érhető el a daganatos beteg állapotában.
Targeted because the medications affect the defective genes or their defective products, thus, they do not directly destroy the tumour, but eliminate the stimulus regulating the pathological cell division. Thus, in many cases, significant improvement can be achieved in the condition of the cancer patient.
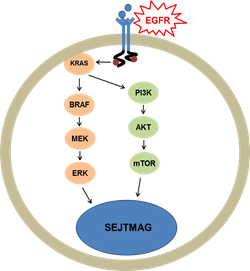
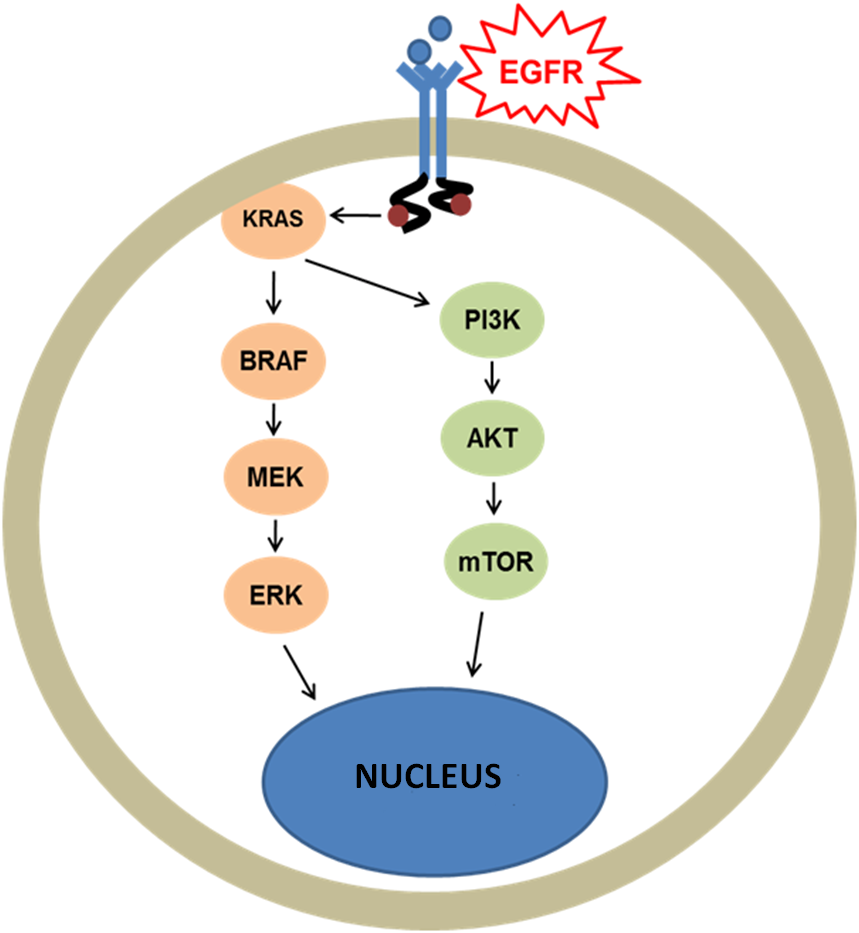
Az EGFR (Epidermal growth factor receptor) egy olyan receptor fehérje, amely a sejtek felszínén található. Ehhez a receptorhoz különböző kis molekulák (elsősorban növekedési faktorok) kapcsolódnak, amelyek a receptor aktiválódását idézik elő. Az aktiválódott receptor jeleket küld a sejt belsejébe, melyek olyan gének aktiválódását eredményezi, amik végső soron sejtosztódáshoz, sejtnövekedéhez, érhálózat fejlődéséhez és áttétképződéshez vezetnek. Számos folyamat vezethet a normálistól eltérő receptor-aktivációhoz. Ezek közé tartozik a receptor túltermelődése, különböző (fent említett) mutációk kialakulása, illetve egyéb mechanizmusok. Az EGFR abnormálisan magas szinten található sokféle típusú rákos sejt felszínén.
EGFR (Epidermal growth factor receptor) is a receptor protein found on the surface of cells. Different small molecules (mainly growth factors) bind to this receptor thus activating it. The activated receptor sends signals into the cell which lead to the activation of genes and, finally, to cell division, cell growth, angiogenesis, and metastasis formation. Several processes can lead to abnormal receptor activation including receptor overproduction, different mutations (mentioned above), and other mechanisms. Abnormal high levels of EGFR can be found on the surface of many types of tumour cells.
Az utóbbi időben számos EGFR gátló anyagot fejlesztettek ki, ami gátolja a jelátviteli útvonalakat megnövelve ezzel a tumoros beteg túlélését. Ezek olyan gyógyszerek, melyek az EGFR receptorhoz kapcsolódnak, ami annak inaktiválódását eredményezi, ez pedig az EGFR jeladás gátlásához, azaz a sejtosztódás, áttétképződés stb. megállásához vezet. Éppen ezért az EGFR gén bizonyos régióinak diagnosztikája elengedhetetlen a megfelelő, hatásos tumorterápia kiválasztásához. Ezek a gyógyszerek nem hatásosak azonban, ha az EGFR jelátviteli útvonal következő tagjaiban (KRAS, NRAS, BRAF, PIK3CA) mutáció található.
Recently, several EGFR inhibitors have been developed that inhibit signalling pathways, improving the survival rates of cancer patients. These medications bind to the EGFR receptor and inactivate it, thus leading to the inhibition of EGFR signalling and halting cell division, metastasis formation, etc. Therefore, the diagnostics of certain regions of the EGFR gene is essential for the selection of an appropriate, efficient tumour therapy. However, these medications are ineffective if a mutation is present in the KRAS, NRAS, BRAF, PIK3CA members of the EGFR signalling pathway.
A gén vizsgálata nem-kissejtes tüdőrák (NSCLC) esetén javasolt.
Analysis of the gene is recommended in cases of non-small cell lung cancer (NSCLC).
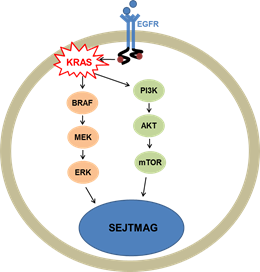
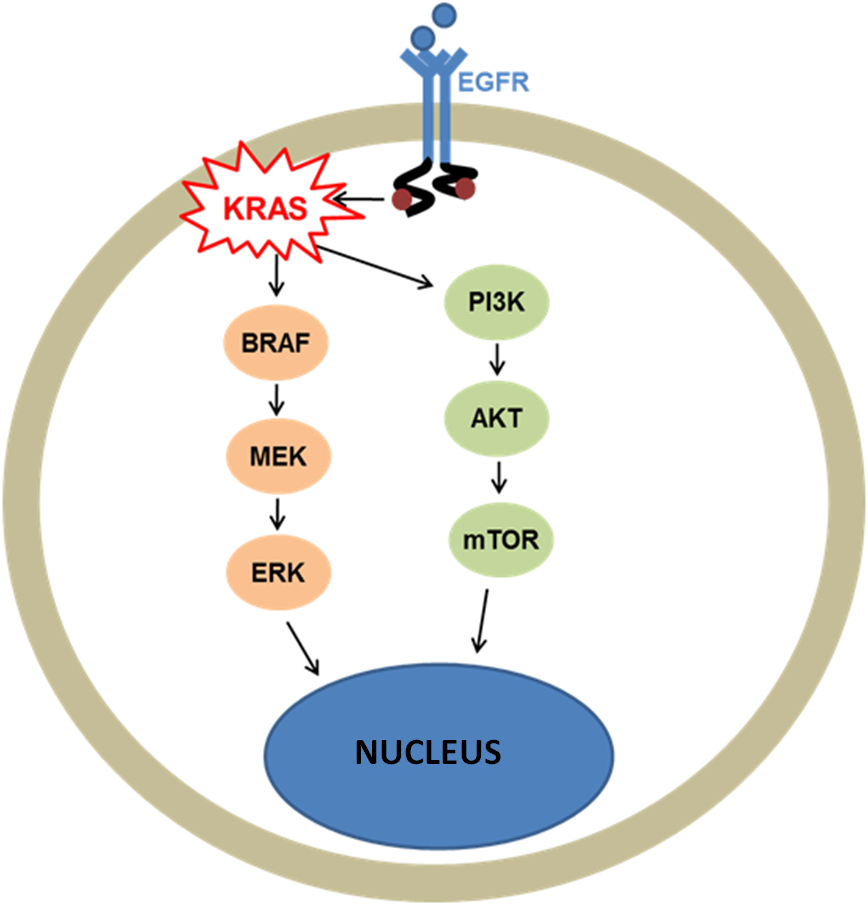
Jelenleg a vastagbéldaganatok és a nem-kissejtes tüdődaganatok kezelésének leghatékonyabb módja az EGFR jelátviteli útvonalat célozza meg, annak különböző tagjait gátolva. A RAS gének által kódolt fehérjék kulcsszereplői az EGFR jelátviteli útvonalnak, aktiváló mutációjuk jelenléte azonban biztos rezisztenciát jelent az anti-EGFR terápiában. A RAS gének közül a leggyakrabban a KRAS gén mutációi fordulnak elő, ezért ajánlott az összes CRC-s és NSCLC-s beteg rutin tesztelése erre a génre. Amennyiben a KRAS illetve NRAS gén mutáció-mentes, úgy az anti EGFR terápia hatásos lehet.
At present, the most efficient therapy of colorectal cancer (CRC) and non-small cell lung cancer (NSCLC) targets the EGFR signalling pathway by inhibiting its different members. The proteins encoded by the RAS genes are key players in the EGFR signalling pathway, and the presence of activating mutations in them indicates a definite resistance to anti-EGFR therapies. KRAS mutations are the most common among RAS mutations; thus, routine screening of all CRC and NSCLC patients is recommended for this gene. If the KRAS and the NRAS genes are mutation-free, the anti-EGFR therapy can be efficient.
A gének vizsgálata elsősorban vastag- és végbélrák (CRC), valamint nem-kissejtes tüdőrák (NSCLC) esetén javasolt.
Analysis of the gene is recommended mainly in cases of colorectal cancer (CRC) and non-small cell lung cancer (NSCLC).
A B-RAF gén szintén az EGFR jelátviteli útvonal tagja, és a daganatok ~7-8%-ban mutáns: melanómák ~45%-ban, pajzsmirigyrákok ~40%-ban, vastagbél daganatok 15%-ban kimutatható a mutációja. Eddig több, mint 100 különböző mutációját írták le ennek a génnek, de a leggyakoribb a 600-as pozícióban található (V600E), ami az összes mutációk több, mint 90%-a. A BRAF V600E mutációja következtében a sejtek növekedési faktortól független, kontrollálatlan növekedése következik be, ezért ennek a jelenlétében hatástalanok maradnak az EGFR-gátló gyógyszerek.
The B-RAF gene, which is also a member of the EGFR signalling pathway, is mutant in about 7-8% of tumours: mutations of this gene can be detected in ~45% of melanomas, ~40% of thyroid cancers, and 15% of colon cancers. Up to now, more than 100 different mutations of this gene have been described, but the most frequent is found in position 600 (V600E), which represents more than 90% of all mutations. Due to the BRAF V600E mutation, cells begin to grow in an uncontrolled way that is independent of the growth factor; thus, in the presence of this mutation EGFR inhibitor medicines are ineffective.
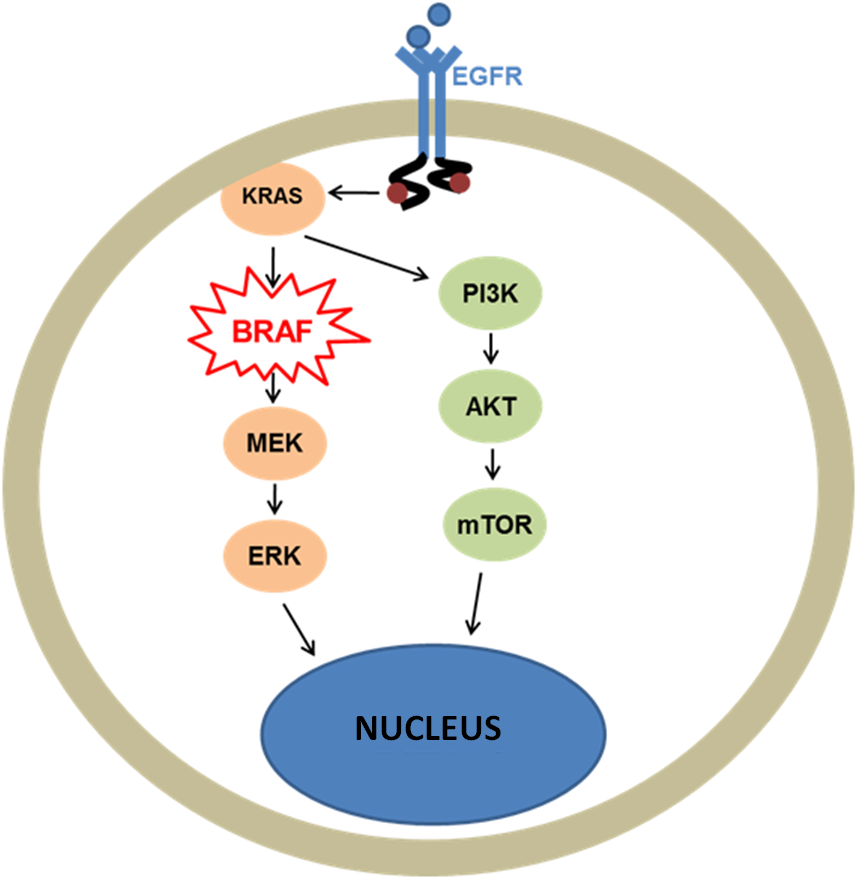
A gén vizsgálata elsősorban melanóma, pajzsmirigyrákok, valamint vastagbél daganatok esetén javasolt.
Analysis of the gene is recommended mainly in cases of melanoma, thyroid cancer, and colon cancer.
A PIK3CA nevű gén a foszfatidilinozitol-3-kináz (PI3K) katalitikus alegységét (p110) kódolja. A foszfatidilinozitolok-3-kinázok olyan jelátviteli útvonalak irányításában vesznek részt, amelyek felelősek a sejtek osztódási, túlélési, adhéziós és mozgási folyamataiért. Ezek a folyamatok hibás működésük esetén daganatképződést eredményezhetnek. A hibás működés kiváltó oka lehet többek között a PIK3CA génben bekövetkező aktiváló mutációk egyike, melyek jelenlétét sok daganattípus (vastagbél-, mell-, gyomorrák és bizonyos agytumorok) esetén kimutatták. A PIK3CA mutációs státuszának szintén fontos szerepe lehet a célzott tumorterápiában, mivel a mutáció jelenléte rezisztenciát kölcsönöz az EGFR inhibitorokkal szemben.
The PIK3CA gene encodes for the catalytic subunit (p110) of phosphatidylinositol-3-kinase (PI3K). Phosphatidylinositol-3-kinases participate in the regulation of signalling pathways that are responsible for processes involved in cell division, survival, adhesion, and movement. Improper functioning of these processes may lead to tumour formation. Erroneous functioning may be caused, among others, by an activating mutation in the PIK3CA gene, which has been detected in many types of tumours (colon, gastric, and breast cancer, and certain brain tumours). The PIK3CA mutational status plays an important role in targeted tumour therapy since the presence of the mutation confers resistance to EGFR inhibitors.
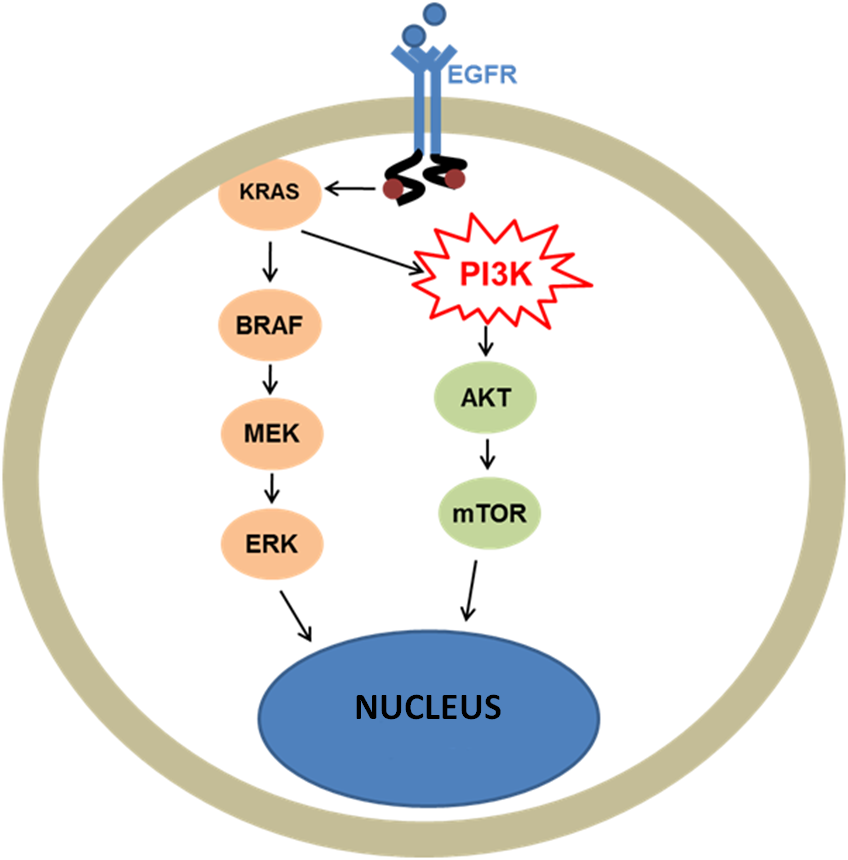
A gén vizsgálata vastagbél-, mell-, gyomorrák és bizonyos agytumorok esetén javasolt.
Analysis of the gene is recommended in cases of colon, gastric, and breast cancer, and in certain cases of brain tumour.
A gén vizsgálata gasztrointesztinális sztróma tumoroknál (GIST), agydaganatoknál (glióma), a májrákok egyik típusánál (hepatocelluláris karcinóma; HCC), a vesesejtes daganatoknál, krónikus mieloid leukémiánál (CML) és a melanomák esetén javasolt.
Analysis of the gene is recommended in cases of gastrointestinal stromal tumours (GIST), brain tumours (glioma), a type of liver cancer (hepatocellular carcinoma; HCC), renal cell carcinoma, chronic myeloid leukaemia (CML), and melanomas.
A KIT-mutáns daganatok hatékonyan kezelhetőek, a célzott terápiához kétféle gyógyszer alkalmazása merülhet fel: a Bcr-Abl tirozin-kináz-gátlók a krónikus mieloid és az akut limfoid leukémia, valamint a GIST-betegek esetében használhatók, egy másik típusú receptor tirozin-kináz-gátlóval pedig azokat a GIST-betegeket lehet kezelni, akik már ellenállóvá váltak a Bcr-Abl tirozin-kináz-gátlóval szemben.
KIT-mutant tumours can be treated efficiently using two types of medicines for targeted therapy: Bcr-Abl tyrosine kinase inhibitors for chronic myeloid and acute lymphoid leukaemia and GIST patients and another type of receptor tyrosine kinase inhibitor to treat those GIST patients who have already become resistant to the Bcr-Abl tyrosine kinase inhibitor.
Magában foglalja az EGFR, a KRAS, az NRAS, a BRAF és a PIK3CA gének diagnosztikáját.
Includes the analysis of the EGFR, KRAS, NRAS, BRAF, and PIK3CA genes.
Társadalmakként változó mértékben az emberek gyomrában megtalálható a Helicobacter pylori nevű kórokozó, ami az esetek túlnyomó részében semmilyen problémát nem jelent. Ugyanakkor egyes esetekben idült gyomorgyulladást, gyomorfekélyt okoz, valamint összefüggésbe hozzák a gyomorrák, illetve a gyomornyálkahártyából kiinduló limfóma kialakulásával. Ezért azon betegek esetében, akiknél a kezelő orvos is úgy ítéli meg, tanácsos a baktérium kiirtása, amely egy intenzív és mellékhatásoktól sem mentes antibiotikum és más gyógyszerek kombinációjával valósítható meg. A kezelés azonban nem mindig sikeres, mert a baktérium antibiotikum rezisztenciával rendelkezik, ami csak a kezelés végére válik nyilvánvalóvá. Mindezt azonban meg lehet előzni a szövettani minta további vizsgálatával, ahol a baktérium antibiotikum (clarithromycin) rezisztenciáját egy genetikai vizsgálattal ki lehet mutatni. Ez információt ad az orvos számára, hogy más gyógyszerkombinációval kezdje a kezelést, csökkentve a hatástalan kezelés okozta mellékhatásokat, illetve annak költségeit. A vizsgálat a gyomorbiopsziás minta szövettani vizsgálati blokkjából történik.
To an extent varying according to populations, the pathogen Helicobacter pylori is present in the stomach of people, causing no problem at all in most of the cases. However, in some cases it can cause chronic gastritis, ulcer, and is associated with the development of gastric cancer and gastric mucosa-associated lymphoid tissue (MALT) lymphoma. Therefore, if deemed necessary by the physician, it is recommended to eradicate the bacterium; this is achieved with an intensive therapy - not without side effects - using a combination of antibiotics and other medicines. However, the eradication therapy is not always successful because the bacterium may be resistant to the antibiotic, which becomes evident only after the treatment. Further analysis of the tissue sample can prevent this; the bacterium’s antibiotic resistance (clarithromycin) can be detected with a genetic test. This provides information for the physician to use a different combination for the treatment thus avoiding the side effects and costs of an ineffective treatment. The test is performed using the tissue block of the gastric biopsy.

